Neste artigo será relatado a Termodinâmica e o trabalho de um gás especial. A termodinâmica é a área da física que estuda a transação de energia térmica em energia mecânica ou vice-versa. Um ocorrido importante de se falar sobre esse tema é que está intimamente conectado ao trabalho de uma força, bem como a temperatura, energia interna de um gás perfeito e o volume.
Podemos calcular o trabalho da força realizada pelo gás, no estudo da termodinâmica, existindo este determinado gás. Para isso, imagine um vaso com um embolo retirável na parte superior (como uma seringa por exemplo), de uma maneira em que este possa se mover sempre que preciso.
O trabalho de um gás na termodinâmica
Quando aplicada uma força F sobre o embolo esta pode ser expressa pela equação F = P . A, onde P é a pressão realizada sobre a área de contato (A).
Sabemos que ele é descrito pelo produto entre a força e a variação do espaço promovida pelo mesmo sobre o trabalho de uma força, logo temos que:
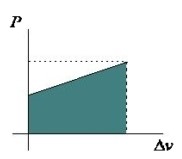
Pode-se também, calcular o trabalho por meio da área do gráfico expresso no plano P x Δv.
Observe também a figura a seguir para ficar mais claro:
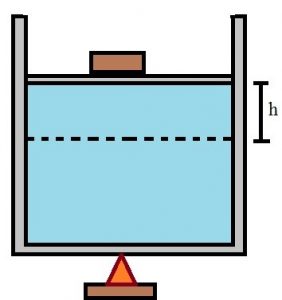
Essa figura ilustra um cilindro com gás em seu interior que se trata de uma variação de temperatura.
O que ocorre?
O êmbolo desse cilindro pode mover-se livremente e sem atrito. O cilindro da figura contém uma massa de gás ideal. O peso diante esse êmbolo conserva constante a pressão no interior do cilindro.
As moléculas do gás recebem energia térmica e começam a movimentar-se, gerando uma expansão que move o êmbolo para cima a uma altura h. Quando esse sistema é submetido a um aumento de temperatura.
Sempre que uma força cria o deslocamento de um corpo, ela realiza trabalho. Esse tal deslocamento ocorreu em consequência de uma força F que agiu sobre o êmbolo. O trabalho feito pela força F é dado relatado equação:
τ = F . h
A pressão é dada pela fórmula:
P = F
A
que pode ser reescrita como:
F = P . A
Sendo:
P – pressão;
F – Força;
A – Área em que a força é exercida.
Obtém-se a expressão que conecta o trabalho realizado pelo gás com a variação do volume gerada por ele ao ser submetido a uma fonte de calor. Substituindo a força na equação anterior, Observe:
τ = P . A. h
A variação de volume é dada pelo produto da área pela altura, assim:
ΔV = A . h
Portanto:
τ = P . ΔV
Para transformações isobáricas a equação obtida é válida somente para os casos em que a pressão é mantida constante.
O trabalho realizado pelos gases
O trabalho realizado por um gás também poderá ser calculado a partir de um gráfico da pressão em função do volume. O gráfico da pressão P em relação do volume V permitirá o cálculo do trabalho realizado pelo gás
A área compreendida entre a reta que representa a variação das duas grandezas e o eixo dos volumes é igual ao trabalho realizado pelo gás:
A = τ
Essa propriedade do gráfico P x V poderá ser prolongada para qualquer tipo de transformação gasosa, não apenas a isobárica.
O vapor a alta pressão gerado durante o aquecimento da água faz com que as pás das turbinas do gerador movam-se, gerando energia elétrica esse fato de um gás conseguir realizar trabalho é aproveitado para a geração de energia elétrica nas usinas termelétricas.
Sendo assim, podemos perceber a extrema importância do estudo da termodinâmica e seus gases especiais no campo da física quântica, esse artigo retrata toda a descrição dessa vertente onde poderá ser utilizado para material de estudo aos estudiosos.







Comentar